根據內政部統計,至2024年第1季,全台65歲以上人口高達415萬人,已佔總人口的17.8%,國家發展委員會更推估至2025年,台灣65歲以上人口比率即將超越20%。
在此同時,最新2023年住宅資料統計彙報也顯示,全國65歲以上老年人口獨自居住之總住宅戶數達69.5萬宅,其中多數為一名老人獨居,約為52.9萬宅,相較於2012年之36.6萬宅,10年間增幅逾九成。
KPMG畢馬威不動產顧問公司董事總經理陳文正表示,老化海嘯已到,地產需求快速上升,已成收益性不動產市場新星,而政府和民間機構整合資源,補強不足之處,也刻不容緩。
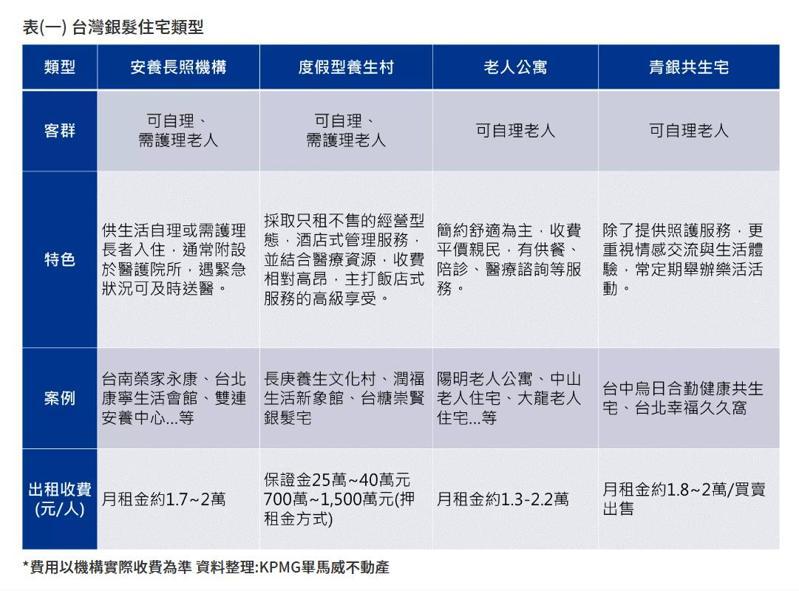
他表示,隨著老人人口快速增加,台灣養老地產也多元發展,從過往單一以醫療照護為主的機構,轉型為服務導向的度假式養生村、價格合理的老人公寓,創新青銀共居宅以及政府推動的社會住宅,都是目前台灣養老居住的新選擇。
另外,在資產活化的趨勢下,近年也有業者將舊有旅館改造成高齡友善的出租宅。
像是位於台北捷運中山站和台北車站的「幸福久久窩」,利用原有的旅館改建,降低土地開發建設的成本,進而大幅下調租金,同時引入高雄醫學大學附設中和紀念醫院建置的智慧醫療裝置,透過「遠距健康管理」的方式,打造在地化且平價的養老宅,是後續值得關注的養老房地產新星。
國營台糖公司也看準銀髮住宅的商機,在台南建立「崇賢銀髮宅」,該案已於2023年12月竣工,將由專業團隊負責經營,目前預計月租金在2至3萬元,設備含有合院中庭、多功能活動空間、體適能室、茶水交誼廳、保健中心和長青教室等多功能共享空間。
KPMG畢馬威不動產顧問公司副總經理林昇恆表示,是高齡化社會的先驅,老年人口比例為全球之首,目前已來到29%,養老地產起步早,也發展出投資模式。
目前日本REITs,「J-REITs」共為58檔,其中含有養老設施(senior facility)就有11檔,其中有一檔HCM,專門以養老設施為資產,股利成長率跟疫情前相比雖下降9.9%,但整體資產淨值則是上升11.7%。
此外,相對於資產取得價格,淨營運收益率在2022及2023年皆為5.5%,高於整體REITs平均收益率4.7%,可見選擇養老房產投資,不僅能為社會貢獻一份力量,能享有穩定現金流和增值空間。
林昇恆表示,未來發展養老房產的方向,建議可考慮利用外部資源來創建一個共融社區。在面對少子化的挑戰時,可以透過活化閒置校區來達到社區安養的目的。
這類似美國「連結大學型退休社區」集合住宅、日本「長期退休計畫」,這些計畫不僅重視地方創生和生涯教育,還為退休長者提供基本的飲食與照護服務,並與校園資源連結,促進跨世代的交流。
另外如日本知名房產公司旗下的養老地產公司,專為60歲以上長者設計的住宅,選址考慮到鄰近的醫療、運動和文化設施,因無需另外規劃公共設施,可降低成本,創造更加親民的租售價格。
公私協力在降低高齡住宅土地開發成本,也是好方向。信義兒福A1公辦都更即是一例,該案由台北市政府與順天建設合作,預計開發完成後,將有60%的住戶為65歲以上的長者,這展現了公私合作達成社區共融養老的可能性。
林昇恆表示,綜觀台灣養老地產現況,多數銀髮住宅僅有單一性提供住居空間的設計,少部分具有完整安養醫療的全方位服務,顯現出現今養老住宅尚缺少系統性,設施服務供應仍需改善的課題。
國人可借鑒國外成功的養老宅案例,由大型企業集團結合旗下醫療院所、設施管理服務及金融保險機構,打造完整保安系統及充分的照護團隊,並提供日常休閒娛樂的需求,定期規劃藝文展或是協助安排例行性之團康活動。
除此之外,也可引進國際具有品牌資源及完整養老地產營運管理經驗之合作廠商,來使高齡者起居能被完整照料,搭配智能醫療產業,多元化經營管理,以實現養老地產品牌國際化的目標。
標題:老化海嘯來了!養老地產成新寵、模式一次看
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。